ヘパリンによる皮膚病変は考えられていたよりも発現率が高い
新規の前向き研究によってヘパリン誘発性皮膚病変の発現率が約7.5%であることが明らかになった。女性、肥満、およびヘパリン治療期間が最長の患者が、最もリスクが高い。
Lisa Nainggolan
【9月29日(ドイツ、フランクフルトアムマイン)】ヘパリン誘発性皮膚病変は考えられていたよりも発現率が高く、特定可能なリスクファクターをもち、遅延型過敏性反応によって生じることが多いことが、新規研究によって明らかになった[1]。Marc Schindewolf博士(ヨハン・ヴォルフガング・ゲーテ大学病院、ドイツ、フランクフルトアムマイン)らは、2009年9月28日に『Canadian Medical Journal』で知見をオンライン報告し、研究結果は「ヘパリン誘発性皮膚病変の概念を変える」ことになるだろうと述べている。
ヘパリン誘発性皮膚病変の発現率と原因はほとんどわかっていないため、ヘパリン(ほとんどの場合はエノキサパリンまたはナドロパリン)の皮下投与を受けた320例の患者を前向きに調査したと、著者らは説明している。それらの患者のうち24例(7.5%)にヘパリン誘発性皮膚病変が発現し、一般的に引用される2%よりもはるかに高い「驚くべき」発現率であったと述べている。
遅延型過敏性反応がすべての症例の原因であり、ヘパリン誘発性皮膚病変のリスクファクターとして次のものが特定された:肥満(ボディマス指数>25mg/kg2;オッズ比4.6)、より長期のヘパリン治療(>9日間;OR 5.9)、および性別が女性(OR 3.0)。
24例すべての患者において皮膚生検、血小板数の測定、および抗血小板第4因子抗体とアレルギーの検査を行ったところ、1例の患者の抗血小板第4因子抗体検査が陽性であった。ヘパリン誘発性皮膚病変の患者におけるヘパリン誘発性血小板減少(HIT)の発現率は高く20%を超えると報告した「既報のデータを、我々のデータは支持しない」と著者らは述べている。
しかし著者らはヘパリン誘発性皮膚病変を「症状」とみなすよう勧めており、「したがって根本的な原因を特定すべきである」と述べている。HITが除外された場合には、未分画ヘパリンの静脈内投与またはフォンダパリヌクスの皮下投与を用いてその後の抗凝固療法を行うことができると著者らは述べている。臨床的にHITが疑われ代替の抗凝固療法が必要な場合には、アルガトロバン、ダナパロイド、またはlepirudinをHITが除外されるまで使用することができると、著者らは結論づけている。
ヘパリン
ご自身の健康問題に関しては、専門の医療機関に相談してください。免責事項もお読みください。
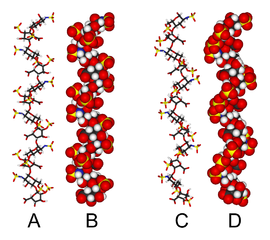 |
| ヘパリンの分子模型 |
ヘパリンの分子模型
ヘパリン (heparin) は抗凝固薬の一つであり、血栓塞栓症や播種性血管内凝固症候群 (DIC) の治療、人工透析、体外循環での凝固防止などに用いられる。ヘパリンの原料は牛や豚の腸粘膜から採取されるが、牛海綿状脳症 (BSE) 発生後の現在は健康な豚から採取されたものがほとんどである。
肝細胞から発見されたため "heparin" と名付けられた(hepato- は「肝の」という意味)が、小腸、筋肉、肺、脾や肥満細胞など体内で幅広く存在する。化学的にはグリコサミノグリカンであるヘパラン硫酸の一種であり、β-D-グルクロン酸あるいは α-L-イズロン酸と D-グルコサミンが 1,4 結合により重合した高分子で、ヘパラン硫酸と比べて硫酸化の度合いが特に高いという特徴がある。この分子中に多数含まれる硫酸基が負に帯電しているため、種々の生理活性物質と相互作用する。
生体内においてヘパリンは細胞表面に存在し、種々の細胞外マトリクスタンパク質と相互作用している。それらのタンパク質の中には、上記の抗凝固作用に関与する凝固系や線溶系のタンパク質の他に、種々の成長因子、脂質代謝関連タンパク質など100を超える種類のタンパク質が含まれ、細胞増殖や脂質代謝にも関与している。
作用機序
アンチトロンビンを活性化し、抗凝血作用能の賦活を通して凝固系を抑制する(APTTを延長する)。アンチトロンビンIIIはトロンビン、第Xa因子およびその他のセリンプロテアーゼを、その活性セリン部位と結合することで阻害する。ヘパリンはこのアンチトロンビンIIIと結合し、構造を変化させて阻害作用を活性化する。トロンビンはヘパリン-アンチトロンビンIII複合体に対して、第Xa因子よりも高い親和性を有する。
トロンビンの阻害には、アンチトロンビンIIIおよびトロンビンの両分子がヘパリンに結合している必要があるが、第Xa因子の阻害では、ヘパリンと第Xa因子の結合は必要でなく、ヘパリンとアンチトロンビンIIIの結合だけでよい。
低分子量ヘパリン (LMWH, Low Molecular Weight Heparin) は出血の副作用が少なく、近年使用頻度が増えてきている。低分子量ヘパリンは、糖鎖が短いためアンチトロンビンIIIとは結合できるが、トロンビンとは結合できないことから、トロンビンの作用を阻害せず、アンチトロンビンIIIとヘパリンの結合のみでよい第Xa因子の作用は阻害する。
薬物動態
ヘパリンは、分子サイズが大きく表面電荷が高いために腸管からは吸収されない。したがって、通常静脈内注射あるいは皮下注射により投与される。ただし、筋肉注射は血腫の危険性が高いため行われない。
未分画ヘパリンの静脈内投与は、血液中からの急速な消失相とそれに続く緩慢な消失相がある。前者は上皮細胞やマクロファージへの結合で、後者は腎臓からの排泄に起因する。静脈内投与では、作用が速やかに現れるが、皮下投与では作用が現れるまで約60分要する。血中半減期は約40?90分である。
低分子量ヘパリンは、皮下注射により投与され、未分画ヘパリンよりも長い半減期(腎排泄のみ)を有する。その消失は一相性であり、血中濃度の予測が未分画ヘパリンよりも容易で、急速な消失がないため投与頻度も少なくて済む。また、低分子量ヘパリンはAPTTを延長しない。
副作用
ヘパリン起因性血小板減少症、血栓症、骨多孔症などが見られる。
Medscape Medical News 2009. (C) 2009 Medscape
|
![]()
![]()

